Koronare Herzkrankheit
Anatomie der Koronararterien
Die
linke Koronararterie entspringt aus dem links-koronaren Sinus und teilt
sich in den RIVA und den RCX auf. In etwa 20% der Fälle teilt sich die
linke Koronararterie nicht in zwei sondern deri Koronararterien auf.
Dieser Ast nennt sich Ramus intermedius.
RIVA. Der RIVA hat zwei Äste - Ramus diagonalis 1 und 2.
Unterteilung - proximales, mittleres und distales Segment. Die Grenze - Abgang vom Ramus diagonalis 1 und 2.
RCX.
Der RCX verläuft im linken Sulcus atrioventrikularis und gibt
normalerweise einen großeren Marginalast und 1-3 Posterolateraläste ab.
Unterteilung - proximales und distales Segment. Die Grenze - Ramus marginalis.
RCA.
Die RCA verläuft im Sulcus strioventricularis dexter und teilt sich in
den RIVP und Ramus posterolateralis dexter. Der größter Ast
entspringt an der Kante zwischen lateraler und inferiorer Wand
des rechten Ventrikels - Ramus marginalis. Andere Äste - Konusarterie,
Sinusknotenarterie, rechtsventrikuläre Äste.
Unterteilung - proximales, mittleres und distales Segment. Die
Trennlinie zwischen dem mittleren und distalen Segment - der
Umschlagpunkt zwischen anteriorer und diaphragmaler rechtsventrikulärer
Herzwand. Die Trennlinie zwischen dem proximalen und mittleren Teil ist
die Mitte der RCA auf der anterioren Wand.
Was bestimmt den Koronarversorgungstyp?
Der Abgangsort des RIVP. 87% - rechtsdominant. 9% - linksdominant. 4% - ausgeglichen (zwei RIVP).
Ätiologie.
Risikofaktoren:
1). Alter.
2). Männliches Geschlecht.
3). Familienanamnese.
4). Hyperchoöesterinämie.
5). Rauchen.
6). Hypertonie.
7). Diabetes mellitus.
8). Bewegungsmangel.
9). Übergewicht.
Pathophysiologie.
"Stenose-Paradox"
- Die milden Stenosen (weniger als 50%) sind gefährlicher in Hinsicht
der Entwickling der instabilen AP oder eines IM (Abriss des Plaques),
als die schweren Stenosen.
Einteilung.
1). Stabile AP - die Schmerzen treten bei bestimmten Belastungen auf und hören nach Belastungsende auf.
2). Instabile AP:
- jede Erstangina
- die Schmerzen in Ruhe, ohne Belastung
- Crescendo-Angina - die Heftigkeit, Dauer und Häufigkeit der Schmerzepisoden nehmen in kurzer Zeit zu
- zunehmender Bedarf an antianginösen Medikamenten.
Sehr selten Prinzmetal-Angina.
CCS-Klassifikation der Angina pectoris.
Stabile AP.
Diagnostik.
Ruhe-EKG. In 50% der Fälle normal. Unspezifische ST-Veränderungen, linksanteriorer Hemiblock, ventrikuläre Extrasystolen.
Belastungs-EKG (Ergometrie).
Die Ergometrie ist keine risikofreie Untersuchungsmethode. Es gibt Kontraindikationen.
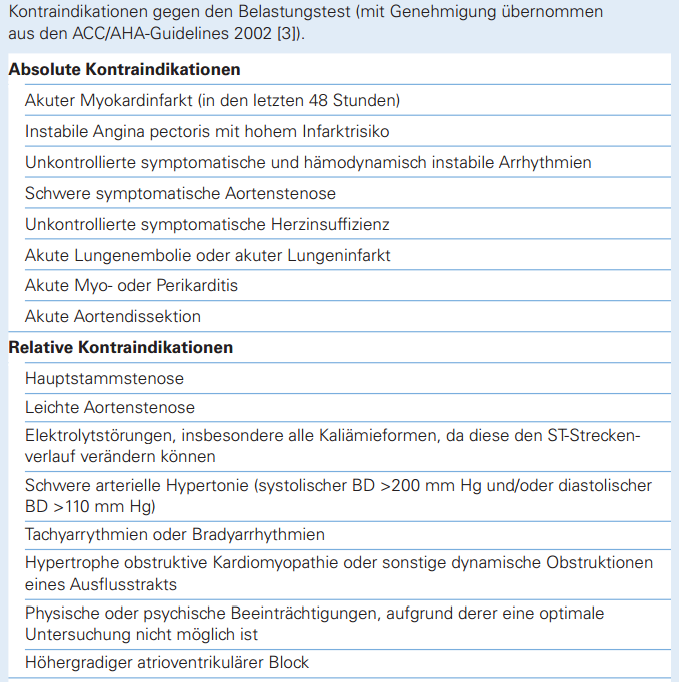
Abbruchkriterien:
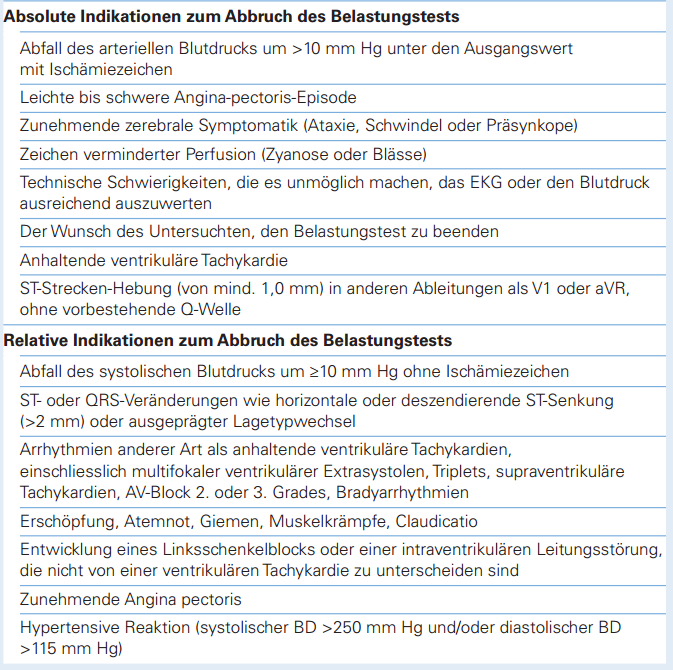
Ausbelastung bei 85% der maximalen altersabhängigen Herzfrequenz (220-Alter).
Ischämiekriterium ist eine horizontale ST-Senkung ab 0,1 mV
(1 mm) in den Extremitätenableitungen und ab 0,2 mV (2 mm) in den
Brustwandableitungen. Eine ST-Senkung mit steilem Anstieg ist nicht
pathologisch. Wenn die ST-Strecke schon im Ruhe-EKG verändert ist, sind
ST-Senkungen unter Belastung nicht eindeutig zu bewerten.
- Präexitationssyndrom
- stimulierter Rhythmus
- LSB oder intraventrikuläre Leitungsverzögerung > 0,12 sek
- ST-Strecken-Senkung von > 1 mm im Ruhe-EKG.
Myokardperfusionsszintigraphie.
Stressechokardiographie.
Koronarangiographie.
Nichtmedikamentöse Therapie.
1). Reduktion des Körpergewichtes.
2). Körperliche Bewegung.
3). Rotwein in Maßen.
4). Schlaf- und Entspannungshygiene.
5). Nikotinkarenz.
6). Fettarme Ernährung.
Die Therapieziele bei stabiler AP:
- zum einen die Ischämiereduzierung, was auch mit der Besserung der
Symptomen einhergeht. Ischämie triggert Arrhythmien und führt zum
Zelluntergang.
- zum zweiten die Aufhalten der Fortschreitung der Erkrankung
(Sekundärprävention, da eine KHK schon besteht).
I. Medikamente (stabile AP).
1).
Betablocker sind Nummer 1. Im Vergleich mit Calciumantagonisten
reduzieren Ischämie besser. Nur bei den absoluten Kontraindikationen
lässt man sich nicht einsetzen (z.B. allergisches Asthma bronchiale).
Aber nützlich sind nur die Herzfrequenz senkende Betablocker ohne ISA
(intrinsische sympathomimetische Aktivität) und in ausreichender Dosis
(Metoprolol 200 mg/d, Bisoprolol 10 mg/Tag, Atenolol 100 mg/Tag).
Die Betablocker mit ISA (Pindolol, Oxprenolol) sind ungünstig.
Kardioselektivität (Beta1-Selektivität) ist unwichtig.
2).
Calciumantagonisten. Sie werden nur als Alternative zu Betablocker
verwendet. Sie senken die Herzfrequenz maximum um 5 % (Betablocker
dagegen um 20-25%). Spezialsituationen:
- Betablocker-Unverträglichkeit bei gleichzeitiger Hypertonie
- Prinzmetal-Angina (extrem selten)
- tachykarde Vorhofflimmern mit Ischämie.
Die Kombination von Betablockern mit Diazepam oder Verapamil sollte
wegen ausgeprägter inotropen Effekt unterlassen werden.
3). Nitraten.
Kurzzeitnitrate (Kapsel oder Spray) verwendet man bei AP-Anfall als Ersttherapie.
Langzeitnitrate spielen nicht so große Rolle. Sie beseitigen nur
Symptome. Aber bei rationeler Therapie soll der Patient beschwerdefrei
sein. Bei Vorliegen der Symptomen unter optimaler Therapie soll eine
Operation oder Dilatation in Frage kommen.
Da eine Gewöhnung besteht, muss man die Nitrate richtig verwenden. Z.B.
Isosorbitdinitrat 80 mg/Tag morgens und mittags, abends NO freisetzende
Molsidomin.
4).
ACE-Hemmer. Sie werden nach IM (auch ohne manifeste Herzinsuffizienz)
verwendet, denn sie das Myokard remodelieren und die Entwicklung der
Herzinsuffizienz vorbeugen.
5). Thrombozytenaggregationshemmer.
Aspirin oder bei Unverträglichkeit Clopidogrel verbessern die Symptome.
6). Medikamentöde Beeinflussung der Risikofaktoren - Hypercholesterinämie, DM, Hypertonie.
Hormonsubstitutionstherapie
bei Frauen nach der Menopause erhöht das kardiovaskuläre Risiko und
soll nur bei hochsymptomatischen Frauen durchgeführt werden.
II. Invasive Interventionen (Herzkatheter).
PTCA (Koronardilatation), häufig mit einer Stent-Einlage:
- bei IM ist besser als Lyse (aber Lyse ist nicht überall verfügbar)
- bei chronische AP keine Überlegenheiten der konservativen Therapie.
Man verwendet aber um von den Symptomen zu befreien.
Drug eluting Stents (Medikamente freisetzende
Stents, beschichtete Stents) - die können die Proliferation der
Neointima supprimieren. Die Ergebnisse - etwa 10% Stents nach 1 Jahr
kommen zum Verschluss (unbeschischtete - etwa 20%).
III. Chirurgische Myokardrevaskularisation.
Die
Operation verlängert das Leben bei einer Hauptstammstenose und bei
3-Gefäß-KHK mit eingeschränkter Pumpfunktion. Für rein symptomatische
Maßnahmen ist die OP nicht geeignet.
A. Fortsetzende Angina pectoris.
B. Anatomie der Stenosen ist so, dass eine chirurgische Revaskularisation bessere Ergebnisse hat:
1). 50% Hauptstammstenose.
2). 3 Gefäß Erkrankung. ...
Akutes Koronarsyndrom.
AKS umfasst drei Krankheitsbilder:
- instabile AP ohne Anstieg von Troponin I oder T
- NSTEMI - Herzinfarkt mit Troponinanstieg, aber ohne ST-Streckung-Hebung
- STEMI - HI mit Troponinanstieg und ST-Hebung.
AKS ohne ST-Hebung
Klinik
Thorakale Schmerzen.
Welche Rolle spielt die Anamnese.
Das Vorliegen der Risikofaktoren erhöhen die Wahrscheinlichkeit des AKS.
Klinische Untersuchung. Rolle.
Klinische Untersuchung dient zur Differentialdiagnose.
Differentialdiagnose.
1). Kardiovaskuläre Erkrankungen:
- Myokarditis
- Perikarditis
- HRSt
- Aortendissektion
2). Lungenerkrankungen:
- Pleuritis
- Pneumothorax
- Lungenembolie
3). Skeletterkrankungen:
- Rippenfraktur
4). Gastrointestinale Erkrankungen:
- Ösophagitis
- Ulcus (Perforation)
- Akute Pankreatitis
5). Weitere Erkrnakungen:
- Herper-Zoster
EKG.
Das EKG bei thorakalen Schmerzen soll innerhalb von 10 min und in 6-12 h geschrieben werden.
Bei AKS ohne ST-Hebung können folgende EKG-Veränderungen auftreten:
- ST-Senkung von >0,1 mV in zwei und mehr Ableitungen
- tiefe negative T-Wellen in den Brustwandableitungen können auf HSS oder RIVA Stenose hinweisen.
EKG bei SM-Träger und bei Schenkelblockbild ist nur eingeschränkt verwertbar.
Das EKG immer mit den früheren EKGs vergleichen.
Biochemische Marker.
Marker der Zellnekrose sind Kreatinkinase und Troponin.
Kreatinkinase. Es gibt drei Isoenzymen:
- CK-MM - Skelettmuskeltyp
- CK-BB - Gehirntyp
- CK-MB - Herzmuskeltyp.
Bei erhöhter Kreatinkinase kann durch Bestimmung der CK-MB zwischen Herz- und Skelettmuskelschäden differenziert werden.
Der Kreainkinase-Anstieg ist in 6 Stunden signifikant, maximal nach 18-20 Stunden und nach 48 Stunden sinkt zur Norm ab.
Die höhe Gesamt CK kann bei i.m. Injektionen, körperliche Anstrengung, Alkoholintoxikationen sein.
Troponin. Es gibt drei Untereinheiten:
Troponin C - bindet Ca++
Troponin I - bindet an Aktin und hemmt die Aktin-Myosin-Interaktion
Troponin T - bindet an Tropomyosin und damit den Komplex an Aktin.
Das Troponin steigt nach 3 Stunden und hält sich hoch 7-10 Tagen.
T1/2 von Troponin?
Falsch positive Erhöhung kommt bei den Patienten mit NI, bei
anderen Krankheiten mit Myokardzellschädigung vor - z.B. Myokarditis,
Lungenembolie, dekompensierte Herzinsuffizienz, Kontusio cordis,
Transplantatanstoßung.
Bei einem Rezidivinfarkt (wenn Troponin hoch ist) ist die Bestimmung von Kreatinkinase besser geeignet.
Marker der Inflammation (CRP) spielen die Rolle in der Prognosebeurteilung.
BNP. BNP hat die prognostische Bedeutung für die Einjahres-Letalität.
Echo. Wandbewegungsstörungen.
Koronarangiographie. Koro ist der Goldstandard zur Diagnose und Schweregradbeurteilung der koronaren Herzerkrankung.
Allgemeinmaßnahmen bei AKS.
- Lagerung mit 30 Grad angehobenem Oberkörper
- Braunüle
- RR-Messung
- 12-Kanal-EKG
Primärtherapie bei AKS.
1). O2 über NS 4-8 L/min
2). Glyceroltrinitrat. 3 Dosen sublingual (0,4 mg) im Abstand von je 5 Minuten.
3). Morphin 3-5 mg i.v.
4). Bei Tachykardie langwirksamer ß-Blocker (Metoprolol 5 mg i.v. langsam)
5). ASS 500 mg i.v.
6). Heparin 70U/kg, max 5000 U, oder Enoxaparin 30 mg i.v.
Bei Übelkeit - MTC.
Bei vagaler Reaktion Atropin 0,5 mg i.v.
Instabile AP und NSTEMI.
Therapie im Krankenhaus.
- antiischämische Therapie
- gerinnungshemmende Therapie
- interventionelle Therapie
- operative Therapie
I. Antiischämische Therapie.
Es gibt drei Klassen von Medikamenten - Nitrate, ß-Blocker, Ca-Antagonisten.
1).
Nitrate.
Zuerst Spray sublingual 2-4 Hub, anschließend im Krankenhaus per Perfusor.
Wirkungsmechanismus - erweiterung der Venen --> es senkt das
Präload, Blutdruck --> Senkung der myokardialen O2-Verbrauch.
Außerdem verbessert es die Blutversorgung der ischämischen Zonen.
Kontraindikationen -- RR syst < 90 mmHg, rechtsventrikulärer Infarkt.
Nebenwirkungen:
- Methämoglobinämie.
2).
ß-Blocker.
Sie sind wirksame medikamenten, besondern bei einer Tachykardie und
höhem RR. Sie senken HF. Das Ziel - 50-60/min. Dosis - Metoprolol i.v.
5 mg, alle 2-5 Min bis zu 3 Dosen, danach orale Weiterbehandlung 50mg
1-2 mal.
Kontraindikationen - AV-Block, Lungenödem.
3).
Ca-Antagonisten.
Nifedipin darf man nur in Kombination mit ß-Blocker.
Diltiazem und Verapamil können eingesetzt werden, wenn die ß-Blocker kontraindiziert sind.
II. Gerinnungshemmende Therapie
- Antithrombine (Heparin) und Thrombozytenaggregationshemmer.
Heparin. Es gibt kleine Studien, die die Senkung des Risiko von Tod
und Myokardinfarkt von 26% bei Heparin zeigen. Daher ist es stark zu
empfehlen. Dosis - zuerst 5000 U, dann 1000U/h. Nach 6 St soll
PTT-Kontrolle laufen.
Niedermolekulare Heparine. Es gibt zwei große Studien zu
Enoxaparin, die die Überlegenheit von Enoxaparin bezüglich
Tod/Myokardinfarkt zeigen.
Hirudin. Bivalirudin. Die Studien sind widersprüchlich. Hirudin senkt
das Risiko von Tod und Myokardinfarkt un 17%, allerdings auf Kosten
einer erhöhten Blutungsrate. Sie werden derzeit nur bei den Patienten
mit bekannter HIT eingesetzt.
ASS. Mit ASS kann das kardiale Risiko auf etwa die Hälfte gesenkt werden. Dosis - 250-500 mg i.v.
Clopidogrel. Was ist besser ASS allein oder die Kombination ASS+Clopidigrel?
Die CURE-Studie zeigt die Überlegenheit der Kombination bezüglich
9-Monates Tod, Myokardinfarkt und Schlaganfall um 20 % (9,3% bei
ASS+Clopidogrel und 11,5% bei ASS).
Dosis - ein Wirkungseintritt von Clopidogrel kann nach 6 St durch Gabe von 300 mg und nach 3 St durch 600 mg erreicht werden.
GP IIb/IIIa Antagonisten. Medikamente -
Abciximab, Tirofiban, Eptifibatide.
Sie senken das kardiovaskuläre Risiko um 9% (GUSTO-IV Studie). Deswegen sind sie gering wirksam.
III. PTCA/Stent
Invasive vs Konservative Strategie.
Die Koronarangiographie mit Intervention ist stark zu empfehlen bei den
Patienten mit AKS ohne ST-Hebung. Die Studien (FRISC II Studie.
TACTICS-TIMI 18 Studie) zeigen, dass das Risiko deutlich gesenkt werden
kann (9,4% versus 12,1% 6-Monates Letalität in der FRISC II Studie).
Das Risiko der interventionellen Therapie bei den Patienten mit
stabiler und instabiler AP ist gleich, wenn man Dual-Hemmungstherapie
(Clopidogrel+ASS) und GPIIb/IIIa einsetzt.
CAPTURE Studie. Die zeigt die Einsatzt des Abciximab bei den Patienten mit AKS:
- bei konservative Therapie die Kombination Abciximab + ASS + Heparin
senkt das kardiovaskuläre Risiko, als nur ASS+Heparin
- bei Intervention senkt Abciximab das Risiko von tod und Myokardinfarkt um 41%.
IV. Chirurgische Myokardrevaskularisation.
Indikationen zur BypassOP bei AKS ohne ST-Hebung.
Es gibt Studien, die zeigen (FRISC II Studie, TACTICS-TIMI 18), dass
die 30-Tages Mortalität ist gleich bei den Patienten mit instabiler AP
oder stabiler AP (beträgt um 2%). Daher sind die Kriterien für eine OP
gleich wie bei den Patienten mit stabiler AP.
Klass I Empfehlung:
- HSS > 50%
- left main equivalent (>70% in proximalem RIVA und RCX)
- refraktorische Ischämie bei maximaler medikamentöse Therapie
Klass IIA:
- proximale RIVA Stenose bei 1-2 Gefäß KHK
AKS mit ST-Hebung (Akuter Myokardinfarkt)
EKG-Veränderungen
EKG-Kriterien für AKS mit ST-Hebung (sie sind auch die Indikationsstellung zur Reperfusionstherapie).
- ST-Hebung > 0,1 mV (1 mm) in mindestens zwei zusammenhängenden Extramitätenableitungen
- >0,2 mV in mindestens zwei zusammenhängenden Brustwandableitungen
- LSB neu.
Die Messung von Biomarkern darf die Therapieentscheidung nicht aufhalten.
EKG-Veränderungen. QRS. ST-Strecke.T-Abschnitt. Mechanismus der Veränderungen.
Q-Zacke. Die Nekrose kann nicht erregen, deswegen dieser Vektor ist
negativ, was in den Exträmitätenableitungen als Q-Zacke und in den
Brustwandableitungen als R-Verlust sich zeigt.
ST-Strecke.
Stadium der Vollerregung. Die ST-Hebung zeigt Ischämie in der
angrenzenden Zone. Die ST-Hebung beginnt vom absteigenden R-Schenkel.
T-Abschnitt. T-Negativierung.
EKG-Stadien des Infarkablaufes.
1). Akutes Stadium - monophasische Erhöhung des ST-T-Abschnittes. Dauer - wenige Stunden bis einige Tage.
2). Folgestadium. Rückbildung der ST-Hebung, die T-Zacke wird spitz-negativ. Dauer - mehrere Tage bis Wochen
3). Endstadium. Normalisierung des ST-T-Abschnittes.
Lokalisation:
- anterior - V1-6
- lateral - I, aVL, V4-6
- inferior - II, III, aVF
- anteroseptal - V1-3
- rechter Ventrikel - V4R, V5R.
Therapie von STEMI.
Bei STEMI muss eine
Reperfusion durchgeführt werden. Es gibt 3 Möglichkeiten:
1). Fibrinolyse.
2). PTCA/Stent.
3). Chirurgische Myokardrevaskularisation.
Time is muscle. Die Zeit bis zur Reperfusion ist viel wichtiger, als Art der Reperfusion.
I. Fibrinolyse.
Indikationen:
- ST-Hebung > 0,1 mV in mindestens zwei zusammenhängenden Extramitätenableitungen
- >0,2 mV in mindestens zwei zusammenhängenden Brustwandableitungen
- LSB.
Absolute Kontaindikationen:
- Schlaganfall in den letzten 6 Monaten
- Trauma, Operation, Kopfverltzung in den letzten 3 Wochen
- Neoplasma oder neurologische ZNS-Erkrankungen
- Magen-Darm-Blutung in den letzten Monaten
- bekannte Blutungsdiathese
- dissezierendes Aortenaneurysma
Relative Kontraindikationen:
- TIA in den letzten 6 Monaten
- orale Antikoagulationstherapie
- Schwangerschaft
- aktives Ulcusleiden
- floride Endokarditis
Die prästationäre Fibrinolyse ist in den ersten 3 Stunden besonders
wirksam und einer primären Katheterintervention bezüglich Reduktion der
Letalität gleichwertig. Die Fibrinolyse darf man
in den ersten 12
Stunden verwenden. Die Fibrinolyse nach 12 St erhöht die Mortalität und wird nicht empfohlen.
Die Kombination von Fibrinolyse + PCI (facilitated PCI) wird derzeit untersucht und bisher nicht empfohlen.
Medikamente - Streptokinase, Alteplase, Reteplase, Tenecteplase.
Streptokinase kostet nicht viel. Man darf nur einmal wegen möglichen Antikörperbildung verwenden.
Therapie mit GP IIb/IIIa Antagonisten in der prähospitalen Phase.
Sie sind nicht zu empfehlen, weil es keine Studie dafür gibt, dass die
die Letalität senken, obwohl sie den Erfolg der PCI verbessern.
"Door-to-balloon" Zeit. Die Zeit zwischen der Übernahme des Patienten und der PCI. Die soll nicht 60 min überschreiten.
II. PTCA. Formen der Ballondilatation.
Perkutane Koronarintervention dient zur Sicherung der Diagnose. Danach
wird versucht, die verschlossenen Stelle mittels eines Führungsdrahtes
zu passieren, um anschließend eine Ballondilatation meist mit
Stentimplantation durchzuführen. In ca. 90% der Fälle gelingt es den
Blutfluß wiederherzustellen.
Terminologie:
- primäre oder direkte Dilatation - Ballondilatation als alleinige Therapie, d.h. ohne Lysetherapie
- Kombination einer Ballondilatation mit einer Fibrinolyse (facilitated PCI).
a) Akut PCI - Beginn mit intravenöse Lyse und sofort anschließender PCI
b) Frühe-PCI - PCI am 1-2.Tag nach einer Lysetherapie
c) Späte PCI - PCI > 2. Tag nach einer Lyse
d) rescue PCI - PCI bei ineffektiver Lyse
Indikation zur Primär Dilatation. Die primäre Dilatation ist die einzige Option zur Revaskularisation bei:
- einer unklaren diagnostischen Situation
- Kontraindikationen zur Lyse
- bei den Patienten mit kardiogenem Schock.
Die Indikationen sind dieselben wie bei Fibrinolyse. Die Zeitgrenze ist unklar. Man gent von 12 Stunden wie bei Lyse aus.
Primäre PCI vs Fibrinolyse. Die PCI ist besser als die Lyse. Sie senkt die Letalität um 25 % im Vergleich mit Lyse.
Der maximale Zeitverlust im Vergleich zum Beginn der Lyse darf 90 min nicht überschreiten.
III. Chirurgische Myokardrevaskularisation.
Indikationen zur Bypass-OP bei AKS mit ST-Hebung.
- erfolglose PCI mit persistierendem Verschluß eines Gefäßes oder persistierender Ischämie
- die Koronaranatomie ist ungeeignet zur PCI (HSS, 3 Gefäß KHK)
- Komplikationen (Perforation)
- Komplikationen des MI (MI, Ventrikelperforation, VSD).
- kardiogener Schock???
ESPRIM-Studie. Molsidomin zeigte keine Reduktion der Mortalität.
Lidokain bei ventr. Extrasystolen. Prophylaktischer Einsatz ist nicht
zu empfehlen. Die hämodynamisch relevante VTs sollen mit ß-Blocker
behandelt werden.
Rechts-ventrikulärer Infarkt.
Klinisches Trias - Hypotension, fehlende Lungenstauung, erhöhter Jugularvenendruck.
EKG - ST-Hebung, V4R.
Echo -Akinesie/Hypokines des rechten Ventrikels, Dilatation, TI.
Vasodilatatoren (Nitrate, Diuretika, ACE-Hemmer) sollten vermieden werden.
Kardiogener Schock. Definition. Therapie.
Definition:
-Systolischer Druck < 90 mm Hg.
-Linksventrikulärer Druck > 20 mm Hg.
-HI < 1,8.
Die IABP führt zur Senkung der Letalität.
Mechanische Infarktkomplikationen. Welche und kurz Therapie.
1). Wandruptur. Sofortige OP.
2). VSD. OP.
3). Mitralinsuffizienz. OP.
Postinfarkt-Perikarditis.
Therapie. ASS-Dosierung soll erhöht werden. NSAID und Steroide sind zurückhaltend einzusetzen.
Mems.
Medikamente bei instabiler AP und NSTEMI:
- antiischämische Therapie (Betablocker, Kalziumantagonist, Nitrate)
- gerinnungshemmende Therapie (Heparin oder Enoxaparin + ASS +
Clopidogrel). Clopidogrel nicht, wenn chirugische Revaskularisation
vorgesehen ist.
Hinterwandinfarkt (inferior). EKG-Veränderungen. - I, II, aVF.
Vorderwandinfarkt - V1-4.
Lateral - I, aVL.
Rechtsherzinfarkt - rechte präkordiale Ableitungen - V4R.
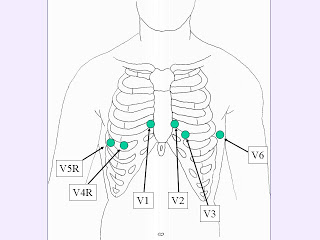
Bei inferiorem Infarkt mit Rechtherzbeteiligung -- Betablocker und Nitrate sind kontraindiziert.