Beatmung
Die Indikationen zur Beatmung aus einer Studie mit 1638 Patienten waren:
- akute respiratorische Insuffizienz - 66%. Subgruppen (jede etwa 10%):
- ARDS
- Herzinsuffizienz
- Pneumonia
- Sepsis
- Operation
- Trauma
- Koma - 15%
- Exarzebationen der COPD - 13%
- neuromuskuläre Probleme - 5%
Ziele
der Beatmung sind 1). Entlastung der Atemmuskulatur und 2). Verhinderung der
lebensbedrolichen Hypoxie (oder respiratorischen Azidose).
Es gibt 5 basische Beatmungszüge:
1). Volume control.
2). Volume assist - der Atemzug wird vom Patienten getriggert.
3). Pressure control.
4). Pressure assist.
5). Pressure support. Es wird auch vom Patienten getriggert. Dann gibt
die Beatmungsmaschine einen eingestellten minimalen Druck (z.B. 10
mbar) und dann der Patient kann selbst noch einatmen.
Der benutzteste Modus ist assist-control ventilation.
Dabei liefern der Respirator ein eingestelltes tidal Volumen, wenn es
von Inspiration des Patienten getriggert wird oder wenn in einer
eingestellten Zeit keine Inspiration stattgefunden hat.
Intermittent mandatory ventilation. Der Arzt stellt eine bestimmte Zahl der Inspirationen des bestimmten tidal Volumens ein. Inzwischen atmet der Patient selbst.
Pressure-support ventilation.
Der Arzt stellt einen bestimmten Druck ein, der bei jeder Inspiration
gegeben wird. Der Druck ist von der Atemfrequenz abhängig (optimal
15-30/min).
Koordinierung zwischen Atemmuskulatur und Beatmug,
Akute respiratorische Insuffizienz geht mit erhöhter Arbeit der
Atemmuskulatur einher. Einerseits wenn die Atemmuskutur nicht entlastet
wird, dann kommt es zur Erschöpfung. Andereseits führt eine
Eliminierung der Atemarbeit zur Atrophie der Atemmuskulatur. Die beste
Koordinierung ist wenn Inspiration bei der Aktivierung der
inspiratorischen Neuronen stattfindet und Expiration - bei der
Aktivierung der expiratorischen.
Bei
assist-control ventilation wird eine Schwelle eingestellt, bei
deren Erreichen wird Inspiration getriggert. Die beträgt -1-2 cm H2O.
Die inspiratorischen Neuronen sind schon aktiviert und nach der
Triggering sie stimulieren die Atemmuskulatur. Die Einstellungen der
Inspiration am Respirator sollen dem Bedarf des Patienten anpassen.
Negative
Folgen der Beatmung. Beatmung kann zur Ruptur der Alveoli führen.
Außerdem passieren Veränderung aus histologischer Ebene. In CT wurde
gezeigt, dass 1/3 der Alveoli sind nicht ventiliert, 1/3 - schlecht
ventiliert und 1/3 - gut ventiliert. Die Luft vom Respirator nimmt
einfach den Weg mit dem niedrigsten Widerstand. Die Beatmung führt zur
Alveolarblutung, Anstieg der Permeabilität und Hyalinmembranformation.
Hickling et al 1990 hat gezeigt, dass niedrieges tidal Volumen bei ARDS um 60% die Letalität sinkt.
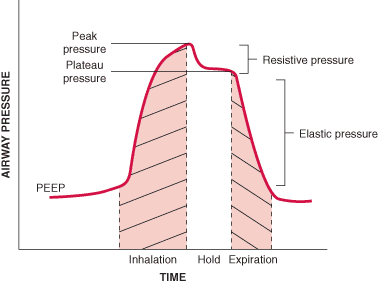
Die Drucke während der Beatmug:
- peak inspiratory pressure
- plateau pressure
- PEEP
Der Gradient zwischen peak inspiratory pressure und plateau pressure zeigt den Widerstand der Atemwegen.
Für
die Trauma der Lunge bei Beatmung viel wichtiger ist transpulmonaler
Gradient (zwischen intraalveolar und Pleurahöhle), als intraalveolarer
Druck an sich selbst. Bei Lungenödem, Abdominal-compartment syndrom ist
der intrapleurale Druck erhöht und der intraalveolare Druck von 35 cm
H2O führt nicht zu Schaden.
Beatmung bei der Bronchoobstruktion.
Peak-Plateau-Gradient
- Gradient zwischen Pmax und Pplateau. Pplateau - der Druck am Ende der
Inspiration. Er kann vermessen werden, indem man die Beatmung nach der
Inspiration stoppt. Der Gradient zeigt die Resistenz der Atemwege. Mit
diesem Gradient kann man unterscheiden zwei Situation mit hohem Pmax -
verminderte Compliance (beide Drücke sind erhöht) und erhöhte Resistenz
(nur Pmax erhöht).
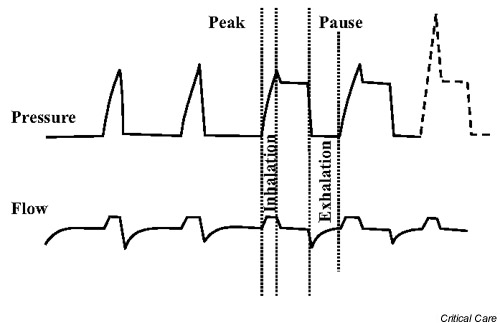
Fig. Peak-Plateau Gradient. Die unterbrochene Linie zeigt den hohen peak-plateau Gradient bei Status asthmaticus.
Auto-PEEP (intrinsic PEEP). Wie
kann man sehen? Auf der Flow-Grafik kann man sehen. Normalerweise kommt
die Flow zum Null am Ende der Expiration. Bei Auto-PEEP gibt es Flow am
Ende der Expiration und beginnt schon die Inspiration.
Wie kann man Auto-PEEP messen? Bei der Expiration wird die Beatmung gestoppt und der Anstieg des Druckes vermessen.
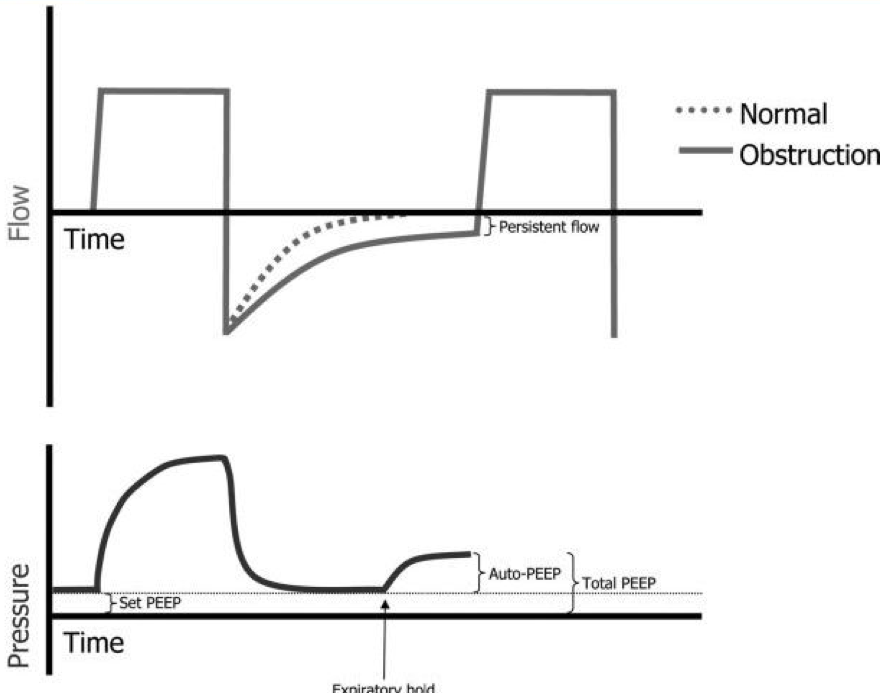
Fig. Auto-PEEP. Der Flow kommt nicht zuz Null-Linie. Die zweite Grafik zeigt, wie kann man den Auto-PEEP vermessen.
Wozu führt der Auto-PEEP?
- Hypoxämie - verminderte ventilation/perfusion matching
- Hypotension - verminderter Preload
- Barotrauma - erhöhter transpulmonarer Druck
- Vermindertes Tidalvolumen bei Druck-kontrollierter Beatmung
- ineffektive Triggering.
Triggering-Probleme bei dem Auto-PEEP.
- Druck-Triggering - der Patient muss den Druck aufbauen höher als Auto-PEEP + eingestellten Schwellendruck
- Flow-Triggering - der Patient muss den Flow aufbauen, die Summe von
Expirationsflow (er kommt nicht zum Null am Ende der Expiration) +
Schwellenflow.
Beatmung bei der Obstruktion. Erstes Ziel - Expiration zu verlängern. Wie kann man das machen?
- I:E Ratio reduzieren bis 1:5
- Tidal Volumen reduzieren
- Frequenz redizieren
- Inspirationsflow erhöhen.
Das kann zur Hypoventilation führen. Aber es ist so besser. Die Hyperkapnie ist gut zu tolerieren.
Aerosol delivery systems.
- jet
- ultrasound
- pMDI - pressurized metered dose inhaler
Patient-Ventilator Interactions.
Interactions - wenn der Patient kann die Parameter der Beatmung beeinflußen. Das kann in drei Punkten passieren.
1). Triggering.
2). Flow (Einatmen). Wenn der eigene Flow des Patienten größer als den
der Maschine, dann kommts es dazu, dass der Patient saugt die Luft.
3). Wann wird das Einatmen beendet.
Dyssynchronie in einer von diesen drei Phasen führt zur übermäßigen Load auf die Atemmuskulatur.
Triggering.
Wenn der Patient Auto-PEEP hat, dann muss er eine größere Muskelkraft entwickeln, um ein Atemzug zu triggern.
Einatmen.
Der
Flow ist etwa 60 l/min. Wenn die Inspiration des Patienten stärker und
der Flow ist nicht groß genug ist, dann kommt es zur Überlastung der
Muskulatur.
Der zu große Flow führt zur Tachykardie. Die Expirationszeit wird kürzer.
Breath cycling (Umschalten zwischen Inspiration und Expiration).
Die
moderne Respiratoren schalten von der Inspiration auf Expiration um,
wenn der Flow 25% vom Peak-Flow beträgt. Bei den Patienten mit COPD
andärt sich der Flow nicht so schnell und die Patienten anfangen,
auszuatmen, während der Respirator noch eine Inspiration macht.
1).
Wenn
die eingestellte Inspiration zu lang ist, dann kommt es zu Problemen
mit
Expiration (Auto-PEEP oder der Patient muss die Muskeln einsetzen, um
auszuatmen). Auf dem folgenden Bild sieht man die Veränderungen der
Druck-Kurve (charakteristische Welle). Der Patient will schon ausatmen,
aber der Respirator macht noch Inspiration. Deswegen steigt der Druck.
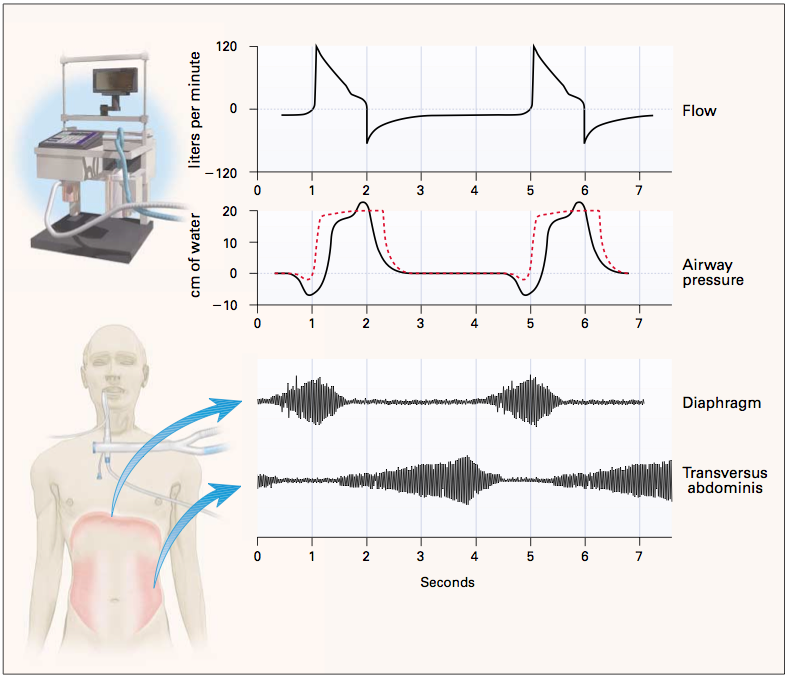
Wenn das eingestellte Einatmen zu kurz ist, dann kommt es zur Doppeltriggering und übermäßigem Load auf die Atemmuskulatur.
Weaning.
Das Stoppen der Beatmung bei der Patienten, die man nicht entwöhnen kann, führt zum Folgendes:
- tidal Volumen 200 ml, AF 38/min (rapid shallow breathing)
- Schwankungen des intrapleuralen Druckes
- Siegerung des Druckes in A.pulmonalis bis 60/30 mm Hg.
Der
Wert Frequenz/tidal Volumen in L (RSBI - rapid shallow breathing index)
kann zeigen, ob der Patient entwöhnt werden kann oder nicht. Je größer
der Quotient ist (rapid shallow breathing), desto unwahrscheinlicher
ist erfolgreicher Weaning. Die Grenze - um 100.
Es
scheint, dass eine allmähliche Reduktion der Unterstützung der
Ventilation führt zur Verkräftigung der respiratorischen Muskulatur und
Entwönung vom Respirator. Die Studien haben allerdings gezeigt, dass
diese Methode die Entwöhnung sogar verlangsamen kann.
4 Arten von Weaning:
1). Intermittierte vielmalige Versuche der Sponaatmung. Die Beatmung
wird ausgeschaltet für 5-10 min pro Tag. Dazu verwendet man T-Stück mit
viel Sauerstoff. Der Patient atmet selbst. Dann wird diese Prozedur
immer öfter durchgeführt, bis der Patient einige Stunde selbst atmet.
Die ist unbeliebt, denn es ist zeit- und personalaufwendig.
2). Intermittent mandatory ventiation. Man senkt die Frequenz der
gegebenen Inspirationen für 2 Stunden pro Tag bis 2--4/min, wenn es
möglich ist.
3). Pressure support. Man senkt den Druck. Der Druck vom 6-8 cm H2O ist
notwendig, um die Resistenz des Tubus zu überwinden.
4). Versuch mit T-Stück für 2 Stunden. Wenn es gelingt, dann wird der
Patient extubiert. Wenn nicht, dann wird er 24 Stunden voll beatmet, um
die Atemmuskulatur erholen zu lassen.
Bei Versuchen mit Spontanatmung geht das Weaning dreimal schneller als intermittent mandatory ventilation.
Vielmalige Versuche am Tag und einmaliger Versuch der Spontanatmung (1
und 4) pro Tag zeigten gleiche Ergebnisse.
IPPV
- intermittent positive pressure Ventilation. Vollkontrollierte
Beatmung. Standard für OP. der Modus braucht volle Sedation und häufig
neuromuskuläre Blockade. Manchmal nennt man CMV (controlled mechanical
ventilation).
Nichtinvasive Beatmung - Unterstützung der Ventilation ohne Verwendung des endotrachealen Tubus.
Noninvasive positive pressure ventilation (NPPV) kann durchgeführt werden mit:
- volume or pressure-cycled ventilation
- bilevel positive airway pressure
- continuous positive airway pressure device
Indikationen:
- akute respiratorische Insuffizienz bei COPD
- Exarzebationen des Astmas
- kardiogene Lungenödem
- chronische RI bei neuromuskulären Störungen, Thoraxdeformationen
Quellen.
1). Tobin MJ. Advances in mechanical ventilation. N Engl J Med 1996.
2). Rabatin. Noninvasive Vetilation. Mayo Clinic Pro 1999.
Mems.
Peak-Plateau-Gradient
-- Gradient zwischen Pmax und Pplateau. Pplateau - der Druck am Ende der
Inspiration. Er kann vermessen werden, indem man die Beatmung nach der
Inspiration stoppt. Der gradient zeigt die Resistenz der Atemwege.
Ursachen
der hohen Resistenz der Atemwege -- 1). Bronchospasmus 2). Vermindertes
Lungenvolumen 3). Obstruktion des Tubus mit Schleim.
Ursachen des verminderten Compliance der Lunge -- 1). Pneumothorax 2) Pleuraergüße 3). Lungenödem.
Auto-PEEP (intrinsic PEEP). Wie kann man sehen? -- Auf der Flow-Grafik kommt der Flow nicht zum Null.
Wozu führt der Auto-PEEP?
- Hypoxämie - verminderte ventilation/perfusion matching
- Hypotension - verminderter Preload
- Barotrauma - erhöhter transpulmonarer Druck
- Vermindertes Tidalvolumen bei Druck-kontrollierter Beatmung
- ineffektive Triggering.
Triggering-Probleme bei dem Auto-PEEP.
- Druck-Triggering - der Patient muss den Druck aufbauen höher als Auto-PEEP + eingestellten Schwellendruck
- Flow-Triggering - der Patient muss den Flow aufbauen, die Summe von
Expirationsflow (er kommt nicht zum Null am Ende der Expiration) +
Schwellenflow.
Beatmung bei der Obstruktion. Erstes Ziel - Expiration zu verlängern. Wie kann man das machen?
- I:E Ratio reduzieren bis 1:5
- Tidal Volumen reduzieren
- Frequenz redizieren
- Inspirationsflow erhöhen.
Das kann zur Hypoventilation führen. Aber es ist so besser. Die Hyperkapnie ist gut zu tolerieren.
Use of sighs -- 3 mal pro Minute (10 cm H2= höher) währen 1 Stunde führt zum Anstieg des PaO2 um 50%.
Z.B. der Patient atmet CPAP 8 cm H2O. Wie kann man sehehn, wie stark
sind die Atemmuskulatur und ob der Patient erschöpft -- Die Druckkurve
ändert sich nicht, weil der Druck in der Pleura wird negativ und in den
Alveolen bleibt so. Aber kann man Vt sehen, je größer, desto kräftiger
ist die Muskulatur. Bei Erschöpfung steigt auch Atemfrequenz.
Etomidate -- häufig Adrenalinsuffizienz.
Dexmedetomidine -- selektive a-2 Agonist, verursacht keine respiratorische Depression.
Sedierung bei PEEP 15, FiO2 100% -- RAAS -3 bis -5. um die
Spontanatmung komplett auszuschalten, den Verbrauch O2 bei
Atemmuskulatur minimiesieren, expiratorische Muskel auszuschalten (sie
vermindern PEEP).
Der Patient ist wach, wenn er 3 von 4 Aufforderungen macht:
- macht die Augen auf auf Ansprache
- bewegt die Augen auf Ansprache
- drückt die Hände
- streckt die Zunge aus.
Wie viel Kalorien pro Tag -- 25-30 kcal/kg pro Tag.
Growth hormone and anabolic steroids in the weaning -- sie spielen
keine Rolle. In einigen Studien war die Gabe von Oxandrolone mit hoher
Dauer der Beatmung assoziiert.
Hb und Weaning -- kein Nachweis, dass Hb > 10 mg/dl verringert die Beatmungsdauer.
|